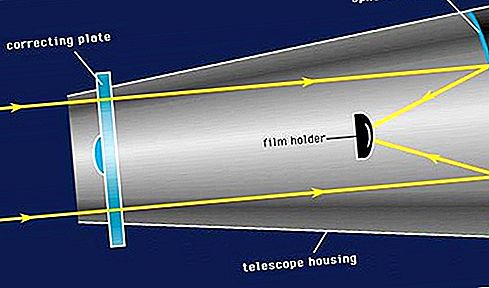
아미드, 암모니아 및 아민과 관련된 두 가지 종류의 질소 함유 화합물 중 하나의 구성원. 공유 아미드는 산의 히드 록 실기 (OH)를 아미노기 (NR 2)로 대체함으로써 형성된 중성 또는 매우 약한 산성 물질 이며, 여기서 R은 수소 원자 또는 메틸, CH 3 와 같은 유기 결합기를 나타낼 수있다). 카르 복실 산 (R'COOH)에서 유도 된 카르 복스 아미드 (R'CONR 2)가 가장 중요한 그룹입니다. 설폰 아미드 (RSO 2 NR 2)는 설 폰산 (RSO 3 H) 과 유사하다.
이온 성 또는 염 유사 아미드는 일반적으로 암모니아, 아민 또는 공유 아미드를 나트륨과 같은 반응성 금속으로 처리하여 제조되는 강 알칼리성 화합물이다.
암모니아로부터 유도 된 공유 아미드는 액체 인 포름 아미드를 제외하고는 고체이며; 5 개 미만의 탄소 원자를 함유하는 것은 물에 용해된다. 그들은 유기 및 무기 물질 모두에 대한 전기 및 용매의 비전 도체입니다. 공유 아미드, 심지어 저 분자량의 아미드는 높은 비점을 갖는다.
단순한 공유 아미드의 실질적인 천연 공급원은 없지만, 폴리 아미드 (폴리머로 불리는 큰 분자를 형성하기 위해 서로 연결된 아미드)는 살아있는 시스템의 단백질로서 많이 존재한다. 단순 아미드는 보통 산 또는 산 할라이드와 암모니아 또는 아민의 반응에 의해 제조된다. 또한 물과 니트릴의 반응에 의해 생성 될 수 있습니다.
공유 아미드의 특징적인 반응은 가수 분해 (물과의 화학 반응)이며, 이것에 의해 산 및 아민으로 전환되고; 이 반응은 강산, 알칼리 또는 효소에 의해 촉매 화되지 않는 한 일반적으로 느리다. 아미드는 또한 니트릴로 탈수 될 수있다. 촉매의 존재하에 수소화 (고온 및 고압에서 수소의 첨가)가 대부분의 카르 복실 산의 아미드를 아민으로 전환시킬지라도, 아미드는 쉽게 산화되거나 환원되지 않는다. 강력한 환원제 인 리튬 알루미늄 하이드 라이드는 아미드를 아민으로 변환시킨다. 아미드와 산 클로라이드 또는 무수물과의 반응은 동일한 질소 원자에 부착 된 2 개의 카보 닐 (CO)기를 갖는 화합물 인 이미 드를 생성한다.
상업적으로 중요한 아미드 중에는 용매, 설파제 및 나일론으로 사용되는 에탄 아미드 (CH 3 CONH 2) 및 디메틸 포름 아미드 HCON (CH 3) 2 로도 불리는 아세트 아미드가있다. 요소 또는 카바 마이드 [CO (NH 2) 2]는 단백질 대사의 최종 산물로서 형성되고 포유 동물의 소변에서 배설되는 결정질 화합물이다. 비료, 동물 사료 및 플라스틱 제조에 사용되는 요소-포름 알데히드 수지로 알려진 고분자 부류의 제조에 사용하기 위해 암모니아와 이산화탄소로부터 대량으로 합성됩니다.


![퀘벡 법 영국 [1774] 퀘벡 법 영국 [1774]](https://images.thetopknowledge.com/img/politics-law-government/5/quebec-act-great-britain-1774.jpg)




![호크스의 큰 잠 영화 [1946] 호크스의 큰 잠 영화 [1946]](https://images.thetopknowledge.com/img/entertainment-pop-culture/6/big-sleep-film-hawks-1946.jpg)