우라늄 (U), 주기율표의 악티 노이드 계열의 방사성 화학 원소, 원자 번호 92. 중요한 핵연료입니다.
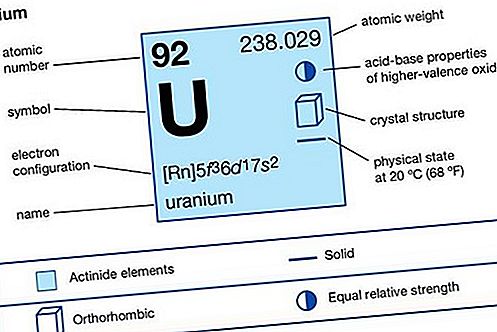

악티 노이드 요소
우라늄 (가장 친숙한)을 포함한 그룹의 구성원은 자연스럽게 발생하며 대부분은 인공입니다. 우라늄과 플루토늄이 모두 사용되었습니다
우라늄은 지구 표면의 백만 개당 약 2 파트가됩니다. 일부 중요한 우라늄 광물은 피치블렌드 (impure U 3 O 8), 우라 닌 나이트 (UO 2), 카르노 나이트 (칼륨 우라늄 바나 데이트), 자폐 물 (칼슘 우라늄 포스페이트) 및 토르 베 나이트 (구리 우라늄 포스페이트)입니다. 핵연료의 원천으로서 이들 및 다른 회수 가능한 우라늄 광석은 모든 알려진 회수 가능한 화석 연료 퇴적물보다 몇 배나 많은 에너지를 함유한다. 1 파운드의 우라늄은 140 만 킬로그램 (3 백만 파운드)의 석탄만큼 많은 에너지를 생산합니다.
우라늄 광석 매장지에 대한 추가 정보와 채굴, 정제 및 회수 기술에 대한 자세한 내용은 우라늄 처리를 참조하십시오. 우라늄 생산에 대한 비교 통계 데이터는 표를 참조하십시오.
우라늄
| 국가 | 광산 생산 2013 (미터 톤) | 세계 광산 생산량의 % |
|---|---|---|
| *견적. | ||
| 출처: 세계 핵 협회, 세계 우라늄 채굴 생산 (2014). | ||
| 카자흐스탄 | 22,574 | 37.9 |
| 캐나다 | 9,332 | 15.6 |
| 호주 | 6,350 | 10.6 |
| 니제르* | 4,528 | 7.6 |
| 나미비아 | 4,315 | 7.2 |
| 러시아 | 3,135 | 5.3 |
| 우즈베키스탄 * | 2,400 | 4.0 |
| 미국 | 1,835 | 3.1 |
| 중국* | 1,450 | 2.4 |
| 말라위 | 1,132 | 1.9 |
| 우크라이나 | 1,075 | 1.9 |
| 남아프리카 | 540 | 0.9 |
| 인도* | 400 | 0.7 |
| 체코 공화국 | 225 | 0.4 |
| 브라질 | 198 | 0.3 |
| 루마니아 * | 80 | 0.1 |
| 파키스탄* | 41 | 0.1 |
| 독일 | 27 | 0.0 |
| 세계 합계 | 59,637 | 100 |
우라늄은 은백색을 띠는 밀도가 높고 단단한 금속 성분입니다. 연성이 있고 가단성이 있으며 높은 광택을 얻을 수 있습니다. 공기 중에서 금속이 변색되고 미세하게 나뉘면 불꽃으로 부서집니다. 상대적으로 열악한 전기 전도체입니다. 우라늄 테트라 클로라이드의 감소에 의해 프랑스어 화학자 유진 멜 치어 펠리 곳으로 천왕성, 금속 자체가 처음 격리 된 후, 최근에 발견 된 행성 (1841)의 이름을 딴 독일어 화학자 마르틴 하인리히 클라 프로트 (UCL에 의해 (1789) 발견했지만 4 과) 칼륨.
1869 년 러시아 화학자 인 Dmitry Mendeleyev의주기적인 체계는 1940 년 최초의 우라늄 원소 넵투늄이 발견 될 때까지 유지 된 가장 무거운 화학 원소 인 우라늄에 주목했다. 1896 년 프랑스 물리학 자 Henri Becquerel은 우라늄에서 발견되었다. 1898 년 프랑스 물리학 자 마리와 피에르 큐리가 처음 사용한 용어 인 방사능 현상. 이 속성은 나중에 다른 많은 요소에서 발견되었습니다. 모든 동위 원소에서 방사성 인 우라늄은 우라늄 -238 (99.27 %, 4,510,000,000 년 반감기), 우라늄 -235 (0.72 %, 713,000,000 년 반감기) 및 우라늄 -234 (0.006 %, 247,000 년 반감기). 이 긴 반감기는 우라늄 함유 암석에서 우라늄의 최종 붕괴 산물 인 납의 양을 측정함으로써 지구의 나이를 판단 할 수있게합니다. 우라늄 -238은 부모이며 우라늄 -234는 방사성 우라늄 붕괴 시리즈의 딸 중 하나입니다. 우라늄 -235는 악티늄 붕괴 계열의 모체입니다. 악티 노이드 요소를 참조하십시오.
우라늄 원소는 독일 화학자 오토 한 (Otto Hahn)과 프리츠 스트 라스 만 (Fritz Strassmann)이 1938 년 후반 느린 중성자에 의해 우라늄이 핵폭발되는 현상을 발견 한 이후 강렬한 연구와 광범위한 관심의 대상이되었다. 이탈리아 태생의 미국 물리학 자 Enrico Fermi는 중성자가 핵분열 산물 중 하나 일 수 있으므로 연쇄 반응으로 핵분열을 계속할 수 있다고 제안했다 (1939 년 초). 헝가리 출신의 미국 물리학 자 Leo Szilard, 미국 물리학 자 Herbert L. Anderson, 프랑스 화학자 Frédéric Joliot-Curie 및 동료들은이 예측을 확인했습니다 (1939). 이후의 조사에 따르면 핵분열 중에 원자 당 평균 2 1 / 2 중성자가 방출되는 것으로 나타났습니다. 그 발견으로 최초의 자립형 핵 연쇄 반응 (1942 년 12 월 2 일), 최초의 원자 폭탄 시험 (1945 년 7 월 16 일), 최초의 원자 폭탄이 전쟁에서 떨어진 (1945 년 8 월 6 일), 최초의 원자력 잠수함 (1955), 최초의 대규모 원자력 발전기 (1957).
핵분열은 상대적으로 드문 동위 원소 우라늄 -235 (유일하게 자연적으로 발생하는 핵분열 물질)에서 느린 중성자로 발생하며, 다양한 용도로 충분한 동위 원소 우라늄 -238과 분리되어야합니다. 그러나, 우라늄 -238은 중성자를 흡수하고 음의 베타 붕괴를 겪은 후, 느린 중성자로 분열되는 합성 원소 플루토늄으로 변형된다. 따라서, 천연 우라늄은 희귀 우라늄 -235에 의해 핵분열이 유지되고 플루토늄이 우라늄 -238의 변형에 의해 동시에 제조되는 변환기 및 종축 반응기에 사용될 수있다. Fissile uranium-233은 자연적으로 풍부한 비 핵분열 토륨 동위 원소 토륨 -232의 핵연료로 사용하기 위해 합성 될 수 있습니다. 우라늄은 또한 합성 트랜스 우라늄 원소가 전이 반응에 의해 제조 된 주요 재료로서 중요하다.
전기 전성이 강한 우라늄은 물과 반응합니다. 산에는 용해되지만 알칼리에는 용해되지 않습니다. 중요한 산화 상태는 +4 (산화물 UO 2 에서와 같이, 테트라 할로겐 (UCl 4 와 같은) 및 녹색 수성 이온 U 4 +에서 와 같이) 및 +6 (산화물 UO 3 에서와 같이, 헥사 플루오 라이드 UF 6 및 노랑 우라 닐)입니다. 이온 UO 2 2+). 수용액에서 우라늄은 우라 닐 이온으로서 가장 안정적이며, 이는 선형 구조 [O = U = O] 2+를 갖는다. 우라늄은 또한 +3 및 +5 상태를 나타내지 만, 각각의 이온은 불안정하다. 용존 산소가 포함되지 않은 물에서도 적색 U 3+ 이온이 천천히 산화됩니다. UO 2 + 이온 의 색은 매우 희석 된 용액에서도 불균형 화 (UO 2 + 가 동시에 U 4 +로 감소 되고 UO 2 2+로 산화 됨) 되기 때문에 알려지지 않았습니다.
우라늄 화합물은 세라믹의 착색제로 사용되어왔다. 6 불화 우라늄 (UF 6)은 25 ° C (77 ° F)에서 비정상적으로 높은 증기압 (115 torr = 0.15 atm = 15,300 Pa)의 고체입니다. UF 6 은 화학적으로 매우 반응성이지만 증기 상태의 부식성에도 불구하고 UF 6 은 우라늄 -235를 우라늄 -238과 분리하는 가스 확산 및 가스 원심 분리 방법에 널리 사용되었습니다.
유기 금속 화합물은 금속을 유기 기와 연결시키는 금속-탄소 결합이 존재하는 흥미롭고 중요한 화합물 그룹이다. 우라노 센은 유기 우라늄 화합물 U (C 8 H 8) 2 이며, 여기에서 우라늄 원자는 시클로 옥타 테트라 엔 C 8 H 8 과 관련된 두 유기 고리 층 사이에 끼워져있다. 1968 년 발견 된 새로운 유기 금속 화학 영역이 열렸습니다.
요소 속성
| 원자 번호 | 92 |
|---|---|
| 원자량 | 238.03 |
| 녹는 점 | 1,132.3 ° C (2,070.1 ° F) |
| 비점 | 3,818 ° C (6,904 ° F) |
| 비중 | 19.05 |
| 산화 상태 | +3, +4, +5, +6 |
| 기체 원자 상태의 전자 구성 | [Rn] 5f 3 6d 1 7s 2 |