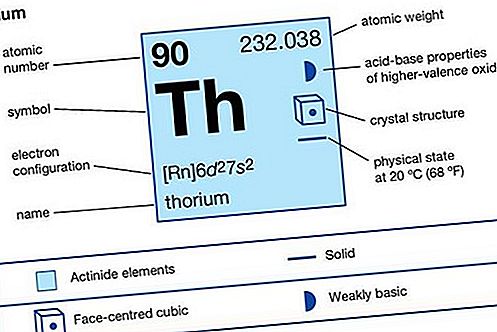
토륨 (Th), 주기율표의 악티 노이드 계열의 방사성 화학 원소, 원자 번호 90; 유용한 원자로 연료입니다. 토륨은 스웨덴의 화학자 인 Jöns Jacob Berzelius에 의해 발견되었습니다 (1828 년). 은백색이지만 공기에 노출되면 회색 또는 검은 색으로 변합니다. 납보다 절반이 풍부하고 지각에서 우라늄보다 3 배 더 풍부합니다. 토륨은 미네랄 모나자이트에서 상업적으로 회수되며 토 라이트 및 토리아 나이트와 같은 다른 미네랄에서도 발생합니다. 토륨 금속은 사 불화물 (ThF 4) 및 이산화물 (ThO 2)의 환원 및 사 염화물 (ThCl 4)의 전기 분해에 의해 상업적인 양으로 생산되었다. 이 요소는 노르웨이 신 Thor의 이름을 따서 명명되었습니다.

악티 노이드 요소: 악티 노이드의 실제 응용
토륨 은 동위 원소 중 하나 인 토륨 -232가 다음과 같이 변환 될 수 있기 때문에 잠재적으로 큰 경제적 가치가 있습니다.
금속은 압출, 압연, 단조, 스웨이 징 및 방사 될 수 있지만, 토륨의 낮은 인장 강도로 인해 연신이 어렵다. 융점 및 비등점과 같은 다른 물리적 특성은 탄소 및 이산화 토륨과 같은 소량의 특정 불순물에 의해 크게 영향을받습니다. 마그네슘과 마그네슘 합금에 토륨을 첨가하여 고온 강도를 향상시킵니다. 2000 ~ 3750 옹스트롬 범위의 파장의 자외선을 측정하기 위해 상업용 광전 전지에 사용되었습니다. 유리에 추가 된 토륨은 굴절률이 높은 유리를 만들어 특수한 광학 응용 분야에 유용합니다. 이전에는 가스 및 등유 램프 맨틀의 구성 요소로 큰 수요가 있었고 전구 및 진공 튜브 용 텅스텐 필라멘트 제조에 사용되었습니다.
토륨의 방사능은 독일 화학자 Gerhard Carl Schmidt와 프랑스 물리학 자 Marie Curie에 의해 독립적으로 발견되었습니다 (1898). 천연 토륨은 방사성 동위 원소, 주로 토륨 방사성 붕괴 시리즈의 모체 인 매우 긴 수명의 토륨 -232 (1.40 × 10 10 년 반감기)의 혼합물입니다. 다른 동위 원소는 우라늄과 악티늄 붕괴 시리즈에서 자연적으로 발생하며 토륨은 모든 우라늄 광석에 존재합니다. 토륨 -232는 느리게 움직이는 중성자를 포획 할 때 핵분열 성 우라늄 -233으로 붕괴되기 때문에 종축 반응기에 유용합니다. 합성 동위 원소가 준비되었다; 합성 액티 노이드 원소 넵투늄에서 유래하는 붕괴 사슬에서 형성된 토륨 -229 (7,880 년 반감기)는 일반 토륨 (토륨 -232)의 추적자 역할을합니다.
토륨은 거의 모든 화합물에서 +4의 산화 상태를 나타냅니다. Th 4+ 이온은 많은 복잡한 이온을 형성합니다. 매우 내화성 물질 인 이산화물 (ThO 2)은 많은 산업 응용 분야를 가지고 있습니다. 질산 토륨은 상업적인 소금으로 사용할 수 있습니다.
요소 속성
| 원자 번호 | 90 |
|---|---|
| 원자량 | 232.038 |
| 녹는 점 | 약 1,700 ° C (3,100 ° F) |
| 비점 | 약 4,000 ° C (7,200 ° F) |
| 비중 | 약 11.66 (17 ° C) |
| 산화 상태 | +4 |
| 기체 원자 상태의 전자 구성 | [Rn] 6d 2 7s 2 |