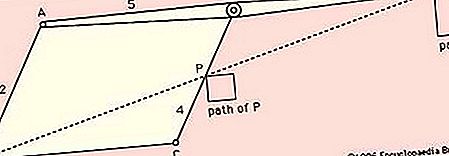
형태, 단일 결합에 대해 그 구성 원자의 기의 회전에 따라서 그 분자 내에 원자의 공간 배열 가능한 무한한 수의 어느 하나.
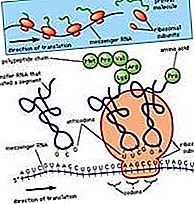
단백질: 인터페이스에서 단백질의 형태
친수성 그룹과 소수성 그룹이 모두있는 다른 많은 물질과 마찬가지로 가용성 단백질은 공기 사이의 계면으로 이동하는 경향이 있습니다.
단일 공유 결합이 2 개의 다 원자 그룹을 연결하는 임의의 분자에 대해 상이한 입체 구조가 가능하며, 이들 각각에서 적어도 하나의 원자는 해당 단일 결합의 축을 따라 놓이지 않는다. 가장 간단한 그러한 분자는 과산화수소의 분자이며, 여기서 2 개의 하이드 록실 기는 산소-산소 결합의 축을 중심으로 서로에 대해 회전 할 수있다. 예를 들어 프로판 (CH 3 -CH 2 -CH 3) 에서와 같이 분자 내에 하나 이상의 이러한 단일 결합의 존재는 그 성질을 바꾸지 않고 상황의 복잡성을 증가시킨다. 시아 노겐 (N≡C-C≡N) 또는 부타 디 인 (H-C≡C-C≡C-H)과 같은 분자에서 모든 원자는 중심 단일 결합의 축을 따라 위치하므로 구별 할 수있는 형태가 없습니다. 있다.
일반적으로, 분자의 모든 구별 가능한 형태는 구조의 다른 부분들 사이의 거리에 따라 변하는 인력 또는 반발력의 작용으로 인해 다른 잠재적 에너지 상태를 나타낸다. 이러한 힘이 없으면 모든 형태는 동일한 에너지를 가지며 단일 결합에 대한 회전은 완전히 자유롭거나 제한되지 않습니다. 힘이 강하면 에너지 또는 안정성이 다른 형태로 크게 다릅니다. 분자는 일반적으로 안정 상태 (낮은 에너지 중 하나)를 차지하고 불안정한 개입에 도달하고 통과하기에 충분한 에너지를 흡수 할 때만 다른 안정 상태로 전환됩니다 형태.
에탄의 분자 내 힘은 예를 들어 엔탈피 및 엔트로피와 같은 열역학적 특성에 대한 미묘한 영향으로부터 유추 될 수있을 정도로 약하다. (에탄의 내부 회전이 심각하게 제한 되더라도 가장 안정된 3 개의 형태는 구별 할 수 없다.) 그러나보다 복잡한 특정 화합물의 분자 구조는 입체 구조에 따라 다른 입체 이성질체 형태가 충분히 안정적이어서 회전에 대한 강한 장벽을 부과한다. 고립되다.